過二硫酸
外觀
此條目需要補充更多來源。 (2024年11月2日) |
| 過二硫酸 | |
|---|---|

| |
| |
| IUPAC名 μ-peroxido-bis(hydroxidodioxidosulfur) peroxydisulfuric acid | |
| 別名 | 過氧二硫酸、過硫酸、馬歇爾酸等 |
| 識別 | |
| CAS編號 | 13445-49-3 |
| PubChem | 24413 |
| ChemSpider | 22822 |
| SMILES |
|
| InChI |
|
| ChEBI | 29268 |
| 性質 | |
| 化學式 | H2O8S2 |
| 莫耳質量 | 194.14 g·mol−1 |
| 外觀 | 無色固體 |
| 熔點 | 65 °C(338 K)(分解) |
| 溶解性(水) | 易溶於水 |
| 相關物質 | |
| 其他陽離子 | 過二硫酸鈉、過二硫酸鉀、 過二硫酸銨 |
| 相關化學品 | 過一硫酸、焦硫酸 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
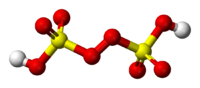
過二硫酸(或稱為「過氧二硫酸」、「過硫酸」或「馬歇爾酸」)是一種硫的含氧酸,分子式為H2S2O8。[1]其結構可以表示為HO3SOOSO3H。雖然過二硫酸分子中的硫的氧化態為+6,但因為該分子中還具有類似過氧根的結構,所以其表現出比硫酸根更高的氧化態。過二硫酸常態下為固體,加熱熔化時易分解。過二硫酸的鹽稱為過二硫酸鹽。
過二硫酸易溶於水並具有吸水性,在熱溶液中易發生水解,先後產生過一硫酸與過氧化氫。過二硫酸具有不穩定性,在室溫下可以緩慢分解,放出氧氣。過二硫酸具有強氧化性,能將氯離子等鹵素離子氧化成鹵素單質、氨氧化成氮氣、將苯胺氧化成苯胺黑,與乙醇、乙醚等有機物作用會發生爆炸。過二硫酸的氧化性弱於過一硫酸。
製備
[編輯]過二硫酸可通過電解硫酸氫鉀獲得過二硫酸鉀,再將該鉀鹽轉化為鋇鹽後經硫酸酸化製備。
- BaS2O8 + H2SO4 → BaSO4↓ + H2S2O8
也可由電解硫酸或將氯磺酸與無水過氧化氫作用製得。過二硫酸鹽則可由電解對應硫酸鹽產生。
用途
[編輯]雖然過二硫酸本身用途並不大,但過二硫酸鹽在工業上用途廣泛,可作為強氧化劑等。
參見
[編輯]參考文獻
[編輯]- ^ Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
