溴化鈷
外觀
| 溴化鈷 | |
|---|---|
| |

| |
| 識別 | |
| CAS號 | 7789-43-7 |
| PubChem | 24610 |
| ChemSpider | 23012 |
| SMILES |
|
| InChI |
|
| InChIKey | BZRRQSJJPUGBAA-NUQVWONBAJ |
| RTECS | GF9595000 |
| 性質 | |
| 化學式 | CoBr2 |
| 莫耳質量 | 218.7412 g/mol(無水) 326.74 g/mol(六水) g·mol⁻¹ |
| 外觀 | 亮綠色晶體(無水) 紫紅色晶體(六水) |
| 密度 | 4.909 g/cm3 (無水) 2.46 g/cm3 (六水) |
| 熔點 | 678 °C(951 K) |
| 溶解性(水) | 無水: 66.7 g/100 mL (59 °C) 68.1 g/100 mL (97 °C) 六水: 113.2 g/100 mL (20 °C) |
| 溶解性 | 77.1 g/100 mL (乙醇, 20 °C) 58.6 g/100 mL (甲醇, 30 °C) 可溶於乙酸甲酯、乙醚和丙酮 |
| 磁化率 | +13000·10−6 cm3/mol |
| 結構 | |
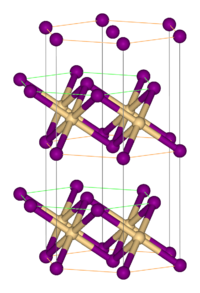
| 晶體結構 | 三方晶系, hP3 空間群:P-3m1, No. 164 |
| 配位幾何 | 八面體 |
| 危險性 | |
| 警示術語 | R:R36, R37, R38 |
| 安全術語 | S:S26, S37, S39, S45, S28A |
| NFPA 704 | |
| 閃點 | 不可燃 |
| 致死量或濃度: | |
LD50(中位劑量)
|
406 mg/kg(大鼠,口) |
| 相關物質 | |
| 其他陰離子 | 氟化鈷 氯化鈷 碘化鈷 |
| 其他陽離子 | 溴化亞鐵 溴化鎳 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
性質
[編輯]無水溴化鈷是綠色晶體,六水合物在100 °C失水,得到二水合物:
- CoBr2.6H2O → CoBr2·2H2O + 4 H2O
二水合物在130 °C完全失水,得到無水物
- CoBr2·2H2O → CoBr2 + 2 H2O
無水物的熔點為678 °C[1][2],在更高溫度和氧反應,形成四氧化三鈷並放出溴蒸氣。
溴化鈷和氨水反應,形成二價的鈷氨配合物,該配合物經過氧化氫氧化,得到穩定的三價鈷配合物二溴化一溴五氨合鈷(III):[3]
- 2 CoBr2 + 8 NH3 + 2 NH4Br + H2O2 → 2 [Co(NH3)5Br]Br2 + 2 H2O
製備
[編輯]- Co(OH)2(s) + 2 HBr(aq) → CoBr2 + 2 H2O
參考文獻
[編輯]- ^ Cobalt Bromide Supplier & Tech Info. American Elements. [2017-08-14]. (原始內容存檔於2015-04-04).
- ^ WebElements Periodic Table of the Elements. [2017-08-14]. (原始內容存檔於2008-05-12).
- ^ Diehl, Harvey; Clark, Helen; Willard, H. H.; Bailar, John C. Bromopentamminocobalti Bromide. Inorganic Syntheses. Inorganic Syntheses 1. 1939: 186. ISBN 978-0-470-13232-6. doi:10.1002/9780470132326.ch66.
- ^ WebElements Periodic Table of the Elements | Cobalt | Essential information. [2017-08-14]. (原始內容存檔於2008-04-02).
- ^ Chemical Properties and Reaction Tendencies 網際網路檔案館的存檔,存檔日期2008-02-19.
- ^ Pilgaard Solutions: Cobalt 網際網路檔案館的存檔,存檔日期2009-01-22.

