用戶:Eland Zhou/朱莉婭-科隆納環氧化
朱莉婭-科隆納環氧化是在三相系統中不對稱的聚亮氨酸催化缺電子烯烴的環氧化物。該反應在1980年由Sebastian Juliá (Instituto Químico de Sarriá, Barcelona, Spain)報道,[1]以及由Juliá和Stefano Colonna (Istituto di Chimica Industriale dell'Università, Milan, Italy)同時做的進一步闡述。[2]

在一般三相條件下,一種查耳酮在聚-L-亮氨酸催化下和過氧化氫進行朱莉婭-科隆納環氧化。圖片摘自朱莉婭等人的論文[2]
原始的反應模式為三相反應,包含了水相、有機相和催化劑相。作為反應物的查耳酮衍生物溶於有機溶劑(例如甲苯或四氯化碳)中,成為有機相。鹼性過氧化氫溶液為水相。反應則發生在既不溶於水相,也不溶於有機相的催化劑聚亮氨酸的表面。兩相甚至均相的改進方法也已開發出來,改進後的反應活性和速率均有顯著提高。[3][4]
該反應是在溫和條件下,立體選擇性地環氧化雙鍵的有效手段,因而在有機合成上具有重大的價值:環氧化物不僅是許多有機合成的中間體,許多天然產物也都是過氧化物。此外,經 Bayer和Evonik等人的工作,該反應已經能夠有效地應用於工業生產。最後,該反應的催化劑聚氨基酸具有類似酶的性質,因而該反應也有助於對生源合成的研究。[5][6]
反應機理
[編輯]朱莉婭-科隆納氧化反應本質上是缺電子碳-碳雙鍵(例如α,β不飽和酮中的碳-碳雙鍵)的不對稱親核環氧化反應。圖 2展示了親核環氧化反應的一般機理,在此反應中,聚亮氨酸作為催化劑控制反應。

過氧化氫陰離子與查耳酮在聚亮氨酸催化劑中形成複合物,然後反應生成過氧化物陰離子中間體。中間體在催化劑結構的控制下迅速關環,立體選擇性地形成產物環氧化物。
三元複合物的生成
[編輯]對該反應的化學動力學研究表明,該反應對含碳-碳雙鍵的底物和過氧化氫負離子都呈現類似酶促反應的動力學,即在底物(或過氧化氫離子)濃度較低時,反應速率與底物(或過氧化氫離子)濃度成正比,而在底物(或過氧化氫離子)濃度較高時,反應速率與濃度無關。兩者所對應的米氏常數分別為Km1=110mM和Km2=30mM。 該研究表明,反應經歷了一個隨機的三元複合物(聚亮氨酸,過氧化氫負離子,底物)的形成過程,並達到穩態。 在形成三元複合物之前,底物和過氧化氫負離子都必須先結合到聚亮氨酸上,雖然兩者結合的先後次序可以顛倒,但在動力學上,過氧化氫負離子先結合的過程更為有利。之後三元複合物繼續反應生成過氧化物陰離子中間體,這是整個反應的決速步。 (圖 3)[5][8]
反應的立體化學
[編輯]在形成過氧化物陰離子中間體之前,所有的反應物必須與催化劑聚亮氨酸結合。催化劑採取α-螺旋構象。反應中,催化劑分子上的四個位於N端附近的酰胺氫與底物形成氫鍵,從而固定了底物乃至中間體的空間取向。雖然也有人提出了其他的模型[9]但Kelly等人的計算表明,NH-2, NH-3 和NH-4 形成了等邊三角形,可以與中間體(過氧化物陰離子)形成氫鍵,從而穩定之。(這一行為類似於酶中的氧陰離子穴。) 雖然含碳碳雙鍵的底物既可以從α-螺旋外側與催化劑結合,也可以從里側與之結合,只有後一種取向才能將NH-4指向過氧化氫負離子,使得最後一步消除反應成為可能。(圖 4)因而,反應是立體專一的。[7]
催化劑
[編輯]聚氨基酸的選擇
[編輯]聚氨基酸的α-螺旋成分越大,反應的立體選擇性也越好。因而用聚亮氨酸或聚丙氨酸做催化劑,可以使反應的立體選擇性最佳。[1]製備催化劑所需的D型和L型光學純的氨基酸均可直接獲得。[10]
催化劑的製備
[編輯]
原始的聚亮氨酸催化劑是由亮氨酸-N-羧酸酐在引發劑(例如胺,醇或水)的作用下聚合形成的。(圖 5) [2]在.三相反應模式里,催化劑必須懸浮在有機相和水相中。[11] – 在兩相反應模式中,通過在反應前用氫氧化鈉活化催化劑,可以提高反應的速率和立體選擇性。催化劑可以被固定在聚苯乙烯,聚乙烯醇或矽油中,形成膠狀物。 [4]
催化劑的二級結構
[編輯]催化劑的活性中心被認為採取α-螺旋結構,其中4-5個N端殘基參與催化反應。雖然催化劑可由非外消旋(可以不是光學純的)亮氨酸製備的,所製備的聚合物分子中也只有那些N端區域保持所有亮氨酸的手性一致的分子,才具有良好的光學活性和催化的立體選擇性。[10]雖然N端具有30個手性一致亮氨酸的催化劑立體選擇性更好[2],由10個手性一致的亮氨酸構成的多肽已經有相當好的立體選擇性了。[10]在後續的研究中發現,用低分子量的氨基酸製備的聚氨基酸具有更好的立體選擇性,這可能是因為單位質量的催化劑中,N端的數目更多。[4]
應用範圍
[編輯]這一缺電子碳-碳雙鍵的環氧化反應最初用於查耳酮的氧化。該反應很快即被運用於其他連有吸電子基的碳-碳雙鍵的環氧化反應,例如α,β-不飽和酮,酯,酰胺。[1][2]反應對不飽和的碸也是有效的。[12]
但有些底物則不適宜用該反應環氧化,包括含有會被過氧化氫破壞的基團的物質,α位含有可解離氫的物質,富電子的碳-碳雙鍵。[10]
這一親核環氧化反應是對親電環氧化反應(例如Sharpless不對稱環氧化反應)的自然補充。
立體選擇性
[編輯]催化劑的結構
[編輯]反應的立體選擇性取決於聚亮氨酸催化劑的α-螺旋結構。如上文所述,雖然N端區域的手性一致是必要的,10個手性一致的亮氨酸構成的多肽已經可以使反應有相當好的立體選擇性了。[10]
非消旋催化劑的手性放大
[編輯]反應立體選擇性只依賴催化劑N端區域的特性可以由以下例子說明:即使是L型過量40%的亮氨酸製備的催化劑也能和光學純的亮氨酸製備的催化劑達到相近的立體選擇性。催化劑和產物光學純度的關係可以近似地用伯努利統計模型描述: een=(Ln-Dn)/(Ln+Dn) 其中L和D是製備催化劑的亮氨酸中L型和D型所佔比例,n是N端起催化作用的氨基酸數目。[5][6]
通過放電實驗模擬地球早期環境,可以獲得包括亮氨酸在內的手性氨基酸,這些氨基酸以非外消旋體的形式存在。類似本反應催化劑的聚氨基酸片段可能來源於咪唑或腈衍生物,這些片段在生命的起源中可能扮演着重要的角色。[5]
改進方法
[編輯]矽基修飾的催化劑
[編輯]矽基修飾的聚亮氨酸可以有效地催化芳香α,β-不飽和酮的環氧化反應。含矽的修飾基團能夠減少催化劑在反應過程中的失活,這對於合成反應來說,是十分有用的。[13]
兩相 (無水) 反應條件
[編輯]在兩相反應的模式下,底物,作氧化劑的尿素-過氧化氫複合物,作鹼的三級胺(例如DBU)溶解在四氫呋喃中,形成一相;固定為膠狀物的聚合物催化劑為另一相。這一改進極大地拓展了反應的適用範圍。[3]
均相反應條件
[編輯]利用可溶性的O,O'-二(2-氨基乙基)聚乙烯醇(diamoPEG)作起始物,可以製得四氫呋喃可溶的三元聚合物。利用這種催化劑可以在均相條件下進行環氧化反應。[4]
相轉移助催化
[編輯]通過加入四丁基溴化銨作為相轉移催化劑,可以大大提高反應速率。這是因為相轉移催化劑的加入可以提高有機相中過氧化氫陰離子的濃度。[14]最初這一改進方法被用於兩相反應模式,但對三相反應同樣起作用。[5][12]
大規模生產
[編輯]在生產中,固定相催化劑已被用在膜式反應器里,催化環氧化反應。目前正在開展將其應用於固定床連續反應器的研究。[11]
合成實例
[編輯]地爾硫䓬的全合成
[編輯]Adger等人利用兩相朱莉婭-科隆納環氧化反應,以固定的聚L-亮氨酸作催化劑,尿素-過氧化氫複合物作氧化劑,DBU作鹼,完成了地爾硫䓬全合成中的關鍵一步。(圖-6)[11]

(+)-黃皮內酰胺的全合成
[編輯]Cappi等人利用朱莉婭-科隆納環氧化反應,以固定在聚乙二醇上的聚L-亮氨酸為催化劑,DABCO-過氧化氫複合物(DABCO-H2O2) 或過氧化氫-尿素複合物為氧化劑,在微型固定床連續反應器中完成了全合成的一步。(圖 7)
該實際應用也從概念上證明了,均相朱莉婭-科隆納環氧化反應是可行的。[15]
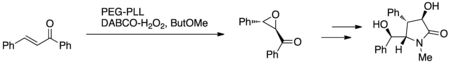
(+)-goniotriol 7, (+)-goniofufurone 8, (+)-8-acetylgoniotriol 9 和 gonio-pypyrone的全合成
[編輯]Chen等人利用兩相朱莉婭-科隆納環氧化反應,以聚L-亮氨酸作催化劑,尿素-過氧化氫複合物作氧化劑,DBU作鹼,完成了一系列從哥那香中提取的內酯的全合成路線中的關鍵一步。這些內酯包括(+)-goniotriol 7, (+)-goniofufurone 8, (+)-8-acetylgoniotriol 9 和 gonio-pypyrone。[16]

參考文獻
[編輯]- ^ 1.0 1.1 1.2 Sebastián Juliá, Jaume Masana, Juan Carlos Vega. “Synthetic Enzymes”. Highly Stereoselective Epoxidation of Chalcone in a Triphasic Toluene-Water-Poly[(S)-alanine] System. Angewandte Chemie International Edition in English. 1980-11, 19 (11): 929–931 [2019-06-25]. ISSN 0570-0833. doi:10.1002/anie.198009291 (英語).
- ^ 2.0 2.1 2.2 2.3 2.4 Juliá, Sebastián; Guixer, Joan; Masana, Jaume; Rocas, José; Colonna, Stefano; Annuziata, Rita; Molinari, Henriette. Synthetic enzymes. Part 2. Catalytic asymmetric epoxidation by means of polyamino-acids in a triphase system. J. Chem. Soc., Perkin Trans. 1. 1982: 1317. doi:10.1039/P19820001317.
- ^ 3.0 3.1 Allen, Joanne V.; Bergeron, Sophie; Griffiths, Matthew J.; Mukherjee, Shubhasish; Roberts, Stanley M.; Williamson, Natalie M.; Wu, L. Eduardo. Juliá–Colonna asymmetric epoxidation reactions under non-aqueous conditions: rapid, highly regio- and stereo-selective transformations using a cheap, recyclable catalyst. J. Chem. Soc., Perkin Trans. 1. 1998, (19): 3171. doi:10.1039/A805407J.
- ^ 4.0 4.1 4.2 4.3 Flood, Robert W.; Geller, Thomas P.; Petty, Sarah A.; Roberts, Stanley M.; Skidmore, John; Volk, Martin. Efficient Asymmetric Epoxidation of α,β-Unsaturated Ketones Using a Soluble Triblock Polyethylene Glycol−Polyamino Acid Catalyst. Org. Lett. 2001, 3 (5): 683. doi:10.1021/ol007005l.
- ^ 5.0 5.1 5.2 5.3 5.4 5.5 Carrea, G; Colonna, S; Kelly, D; Lazcano, A; Ottolina, G; Roberts, S. Polyamino acids as synthetic enzymes: mechanism, applications and relevance to prebiotic catalysis. Trends in Biotech. 2005, 23 (10): 507. doi:10.1016/j.tibtech.2005.07.010.
- ^ 6.0 6.1 Kelly, David R.; Meek, Alastair; Roberts, Stanley M. Chiral amplification by polypeptides and its relevance to prebiotic catalysis. Chem. Comm. 2004, (18): 2021. doi:10.1039/B404379K.
- ^ 7.0 7.1 Kelly, D. R.; Roberts, S. M., The mechanism of polyleucine catalysed asymmetric epoxidation". Chem. Comm. 2004, (18), 2018-2020. doi:10.1039/B404390C
- ^ Carrea, G.; Colonna, S.; Meek, A. D.; Ottolina, G.; Roberts, S. M., "Kinetics of chalcone oxidation by peroxide anion catalysed by poly-L-leucine". Chem. Comm. 2004, (12), 1412-1413. doi:10.1039/B401497A
- ^ Berkessel, A.; Gasch, N.; Glaubitz, K.; Koch, C., "Highly enantioselective enone epoxidation catalyzed by short solid phase-bound peptides: Dominant role of peptide helicity". Org. Lett. 2001, 3 (24), 3839–3842. doi:10.1021/ol0166451
- ^ 10.0 10.1 10.2 10.3 10.4 Bentley, P. A.; Cappi, M. W.; Flood, R. W.; Roberts, S. M.; Smith, J. A., Towards a mechanistic insight into the Julia-Colonna asymmetric epoxidation of α,β-unsaturated ketones using discrete lengths of poly-leucine. Tet. Lett. 1998, 39 (50), 9297–9300. doi:10.1016/S0040-4039(98)02090-5
- ^ 11.0 11.1 11.2 11.3 Adger, B. M.; Barkley, J. V.; Bergeron, S.; Cappi, M. W.; Flowerdew, B. E.; Jackson, M. P.; McCague, R.; Nugent, T. C.; Roberts, S. M., "Improved procedure for Julia–Colonna asymmetric epoxidation of α,β-unsaturated ketones: total synthesis of diltiazem and Taxol (TM) side-chain". J. Chem. Soc.-Perkin Trans. 1 1997, (23), 3501–3507. doi:10.1039/A704413E
- ^ 12.0 12.1 Lopez-Pedrosa, J. M.; Pitts, M. R.; Roberts, S. M.; Saminathan, S.; Whittall, J., "Asymmetric epoxidation of some arylalkenyl sulfones using a modified Julia–Colonna procedure". Tet. Lett. 2004, 45 (26), 5073–5075. doi:10.1016/j.tetlet.2004.04.190
- ^ Yi, H.; Zou, G.; Li, Q.; Chen, Q.; Tang, J.; He, M. Y., "Asymmetric epoxidation of alpha,beta-unsaturated ketones catalyzed by silica-grafted poly-(L)-leucine catalysts". Tet. Lett. 2005, 46 (34), 5665–5668. doi:10.1016/j.tetlet.2005.06.096
- ^ Geller, T.; Gerlach, A.; Kruger, C. M.; Militzer, H. C., "Novel conditions for the Julia–Colonna epoxidation reaction providing efficient access to chiral, nonracemic epoxides". Tet. Lett. 2004, 45 (26), 5065–5067. doi:10.1016/j.tetlet.2004.04.188
- ^ 15.0 15.1 Cappi, M. W.; Chen, W. P.; Flood, R. W.; Liao, Y. W.; Roberts, S. M.; Skidmore, J.; Smith, J. A.; Williamson, N. M., "New procedures for the –Colonna asymmetric epoxidation: synthesis of (+)-clausenamide". Chem. Comm. 1998, (10), 1159-1160. doi:10.1039/A801450G
- ^ 16.0 16.1 Chen, W. P.; Roberts, S. M., "Julia–Colonna asymmetric epoxidation of furyl styryl ketone as a route to intermediates to naturally-occurring styryl lactones". J. Chem. Soc.-Perkin Trans. 1 1999, (2), 103–105. doi:10.1039/A808436J



