同分異構
此條目没有列出任何参考或来源。 (2023年3月10日) |

同分異構物(英語:Isomer)是擁有相同分子式,但結構式卻不相同的多種分子。其彼此間的化學性質並不相同,除非它們擁有相同的官能团(functional groups)。化學中常見的兩種主要的種類為結構異構(structural isomerism或constitutional isomerism)以及立體異構(stereoisomerism)。
历史
[编辑]同分异构现象第一次被注意到是在1827年,当弗里德里希·维勒制备异氰酸的时候,他注意到尽管元素组成与尤斯图斯·冯·李比希在前一年制备出来的雷酸完全相同,但是它们的性质却极为不同。这个发现挑战了当时的主流化学界的理解,当时主流思想认为仅当元素组不同的时候,化合物才会不同。随着更多此类现象被發現,比如維勒在1828年发现尿素与氰酸铵有着相同的原子组成却有着不同的性质,永斯·贝采利乌斯便引进“同分异构”来描述这种现象。
例子
[编辑]丙醇是“同分异构体”的一个简单的例子:它的分子式是C3H8O(或C3H7OH)它的两个同分异构体是1-丙醇(I)和2-丙醇(II)
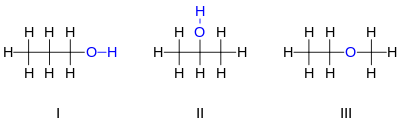
可以注意到两个分子中的氧原子的位置是不同的:在第一个同分异构体中,它是连接在末端碳原子上,而在第二个分子中是连接在中间碳原子上。同分异构体的个数随着原子的个数增长而急剧增加。比如丁醇(C4H10O)就含有4个不同的同分异构体。
在上述例子中,两个同分异构体所有的化学键均为共价键,没有任何一个类型的键在其中一个分子中出现而不在另外一个分子中出现。同样,键的数量也是一样的。根据两个分子的结构我们可以推测它们的化学稳定性很可能是相同或相似的。
然而,另外一个C3H7OH的同分异构体-甲基乙基醚(III),却有着截然不同的性质。和上面两个例子不同的是,氧原子并不是连接着一个碳原子和一个氢原子,而是和两个碳原子相连。因为它没有羟基,上面这个化合物并不是一个醇而是一个醚,因此它的化学性质和其他的醚更加相近。
另外一个有着不同化学性质的同分异构体的例子是黄嘌呤。巧克力中的可可碱中如果两个甲基中的一个移动到双环上的另外一个位置,这个同分异构体就是茶碱了。

分类
[编辑]结构异构
[编辑]在结构异构中,原子或官能团以不同的形式互相连接。
碳链异构
[编辑]官能团不发生改变,仅仅是碳链发生改变。
例:C4H10(丁烷)
位置异构
[编辑]例:C3H7OH
官能团异构
[编辑]相同的原子组成的官能团不同
例:C2H6O
立体异构
[编辑]在立体异构中,键的结构是相同的,但是原子和官能团的空间位置关系却是不同的。
对映异构(手性异构)
[编辑]在对映异构体中,不同的两个异构体是呈镜面对称的。如上图上面两个互为镜像的分子。
非对映异构
[编辑]在非对映异构体中,两个异构分子不呈镜面对称。如上图中上下两个分子。
构象异构
[编辑]在构象异构中,同分异构体之间可以通过化学键的旋转而互相变化。但应该注意到,尽管构象异构体可以被认为是一种非对映异构体,但是从整体来看,它们并不是非对映异构体,因为键的旋转可以使它们形成它们的镜像。
顺反异构
[编辑]顺反异构体之间是不能通过化学键的旋转而互相转化,这是由于例如碳碳双键等不可旋转的键造成的。
其他非對應异构
[编辑]等規(isotatic),間規(syndiotactic),無規(atactic)組態
意义
[编辑]在食品化学,药物化学和生物化学当中,顺反异构体是经常要被考虑到的。而对映异构体在近几十年来成为了药物化学和生物化学关注的焦点,因为在生物有机体当中,我们知道的大部分此类异构体间的转化是有意义的。医药工业和大学里面的研究员们已经把色析法作为一种有效的分离两个同分异构体的办法。然而,这种方法在工业化的环境下是不适用的,因为它们十分昂贵,因此仅当另一个同分异构体有潜在危害的时候才使用。
与构型异构体之间有着不同的化学性质不一样,几何异构体之间通常有着相同的化学性质。然而酶能够有效地区分出一个化合物的几个几何异构体,生物有机体也常常倾向于某一个异构体。一些异构体之间偏振光能力也不同。
除了上述的几种同分异构体,还存在拓扑异构体和同位素异构体。几个拓扑异构体的例子是一些双环化合物和DNA,拓扑异构酶能够使DNA打结改变它的拓扑结构。同位素异构体有着相同数量的同位素取代,但是它们有着不同的位置。在核物理中,核异构体则是原子核的激发态。